Концентрована сірчана кислота: властивості, реакції
Триоксид сірки, як правило, має вигляд безбарвної рідини. Він також може існувати у вигляді льоду, волокнистих кристалів або газу. Коли триоксид сірки піддається впливу повітря, починає виділятися білий дим. Він є складовим елементом такого хімічно активної речовини, як концентрована сірчана кислота. Це прозора, безбарвна, масляниста і досить агресивна рідина. Вона використовується у виробництві добрив, вибухових речовин, інших кислот, в нафтовій промисловості, в свинцево-кислотних акумуляторних батареях в автомобілях.
 Деякі властивості полягає в тому, що молекулярна маса становить 9808. Температура кипіння становить 327 градусів Цельсія, плавлення -2 градуси Цельсія. Сірчана кислота є сильною мінеральною кислотою і одним з головних продуктів хімічної промисловості через її широкого комерційного застосування. Вона утворюється природним чином в результаті окислення сульфідних матеріалів, таких як сульфід заліза. Хімічні властивості сірчаної кислоти (H 2 SO4) проявляються у різноманітних хімічних реакціях:
Деякі властивості полягає в тому, що молекулярна маса становить 9808. Температура кипіння становить 327 градусів Цельсія, плавлення -2 градуси Цельсія. Сірчана кислота є сильною мінеральною кислотою і одним з головних продуктів хімічної промисловості через її широкого комерційного застосування. Вона утворюється природним чином в результаті окислення сульфідних матеріалів, таких як сульфід заліза. Хімічні властивості сірчаної кислоти (H 2 SO4) проявляються у різноманітних хімічних реакціях: При взаємодії з лугами утворюються два ряди солей, в тому числі сульфати. Реагує з карбонатами і гидрокарбонатами з утворенням солей і вуглекислого газу (СО 2 ). На метали вона впливає по-різному, в залежності від температури і ступеня розведення. Холодна і розбавлена дає вихід водню, гаряча і концентрована дає викиди SO 2 . На триоксид сірки (SO 3 ) і воду (Н 2 О) розкладається при кип'ятінні розчин H 2 SO4 (концентрована сірчана кислота). Хімічні властивості включають також роль сильного окислювача.
Помістити потерпілих на свіже повітря. Співробітники екстрених служб повинні уникати при цьому впливу сірчаної кислоти. Оцінити життєві показники, включаючи пульс і частоту дихання. Якщо пульс не виявляється, провести реанімаційні заходи в залежності від отриманих додаткових травм. Якщо дихання є і утруднене, забезпечити респіраторну підтримку. Зняти запачканную одяг як можна швидше. У разі попадання В очі промивати теплою водою принаймні 15 хвилин, на шкіру – промити водою з милом. При вдиханні отруйних парів потрібно прополоскати рот великою кількістю води, пити і самостійно викликати блювоту забороняється. Доставити потерпілих у лікувальний заклад.
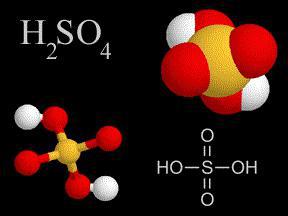
Концентрована сірчана кислота: властивості
Сірчана кислота добре розчиняється у воді, має корозійним впливом на метали і тканини, при контакті обвуглює деревину і більшість інших органічних речовин. У результаті тривалого впливу низької концентрації речовини або короткочасному впливі високої можуть мати місце несприятливі наслідки для здоров'я від вдихання. Концентрована сірчана кислота використовується для виготовлення добрив та інших хімікатів, переробці нафти, у виробництві чавуну та сталі й для багатьох інших цілей. Оскільки вона має досить високу температуру кипіння, вона може бути використана для випуску більш летких кислот з їхніх солей. Концентрована сірчана кислота володіє сильним гігроскопічним властивістю. Її іноді використовують в якості сушильного агента для дегідратації (видалення води хімічним методом) багатьох сполук, наприклад, вуглеводів.Реакції сірчаної кислоти
Концентрована сірчана кислота незвичайним чином реагує на цукор, залишаючи за собою ламкий губчасту чорну масу з вуглецю. Подібна реакція спостерігається при впливі на шкіру, целюлозу та інші рослинні і тваринні волокна. Коли концентрована кислота змішується з водою, виділяється велика кількість тепла, достатню для миттєвого кип'ятіння. Для розведення її слід додавати повільно в холодну воду при постійному помішуванні, щоб обмежити накопичення тепла. Сірчана кислота реагує з рідиною, утворюючи гідрати з різко вираженими властивостями.Фізичні характеристики
Рідина без кольору і запаху в розбавленому розчині має кислий смак. Сірчана кислота є екстремально агресивної при впливі на шкіру і всі тканини організму, при безпосередньому контакті викликає сильні опіки. У чистому вигляді H 2 SO4 не є провідником електрики, однак ситуація змінюється в протилежну сторону з додаванням води.

Пожежна небезпека
Сірчана кислота володіє високою реакційною здатністю до займання дрібнодисперсних горючих матеріалів при контакті. При нагріванні починають виділятися високотоксичні гази. Вона є вибухонебезпечною і несумісною з величезною кількістю речовин. При підвищених температурах і тиску можуть відбуватися досить агресивні хімічні зміни та деформації. Може бурхливо реагувати з водою та іншими рідинами, приводячи до розбризкування.Небезпека для здоров'я
Сірчана кислота роз'їдає всі тканини організму. Вдихання парів може призвести до серйозних пошкоджень легень. Ураження слизової очей може привести до повної втрати зору. Контакт з шкірою може викликати важкі некрози. Навіть кілька крапель можуть бути фатальними, якщо кислота отримує доступ до трахеї. Хронічний вплив може викликати трахеобронхіт, стоматит, кон'юнктивіт, гастрит. Можуть виникнути перфорації шлунка і перитоніт, супроводжувані циркуляторним колапсом. Сірчана кислота є дуже їдкою речовиною, з яких слід звертатися з особливою обережністю. Ознаки і симптоми при впливі можуть бути важкими і включають слинотеча, сильну спрагу, утруднення ковтання, біль, шок і опіки. Блювотні маси, як правило, мають колір меленої кави. Гостре інгаляційне вплив може призвести до чиханию, осиплості голосу, задухи, ларингіту, задишці, подразнення дихальних шляхів і біль у грудях. Кровотечі з носа і ясен, набряк легенів, хронічний бронхіт і пневмонія також можуть виникнути. Вплив на шкіру може призвести до серйозних больовим опіків і дерматиту.Перша допомога
Читайте також
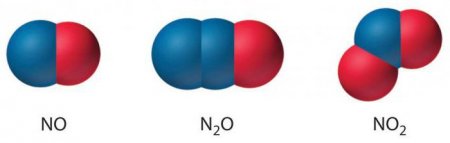
НАУКА
Оксид азоту: формула, властивості, застосування

НАУКА
Скільки в грамі міліграм і навіщо це потрібно знати

НАУКА
Ступінь і константа гідролізу

НАУКА
Діоксид вуглецю: формула, властивості та області застосування

НАУКА
Оксид калію: формула, взаємодія

НАУКА
Кисень: хімічні властивості елемента

НАУКА
Клас небезпеки. Клас пожежної небезпеки, небезпеки речовин, відходів

НАУКА
Сама сильна кислота. Формула самої сильної кислоти






