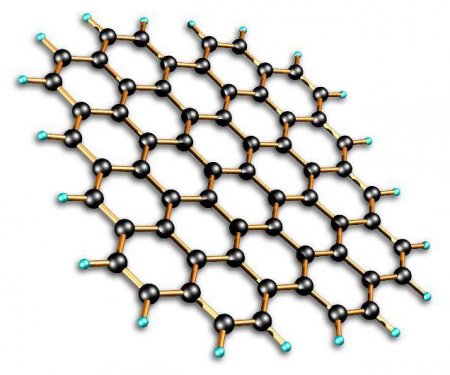
Молекулярна будова речовини
Досить тривалий час вчені створювали теорії і моделі, які б допомагали пояснити основні властивості речовин і матерій, з яких складається навколишній світ.  В ході історії було проведено безліч дослідів, експериментів; були відкриті нові закони і фізико-хімічні властивості матеріалів. Багато в чому це відбувалося завдяки відкриттю понять «молекула» і «атомно-молекулярну будову речовини». Поговоримо про них докладніше в даній статті.
В ході історії було проведено безліч дослідів, експериментів; були відкриті нові закони і фізико-хімічні властивості матеріалів. Багато в чому це відбувалося завдяки відкриттю понять «молекула» і «атомно-молекулярну будову речовини». Поговоримо про них докладніше в даній статті.
Таким чином, незважаючи на те, що певної концепції все ж не було, в ході досліджень почала з'являтися теорія про те, що кожна речовина є різним набором молекул і атомів, які визначають його основні властивості. Вперше термін «молекула» було введено в 1811 році італійським фізико-хіміком Амедео Авогадро. Саме він став зачинателем теорії атомно-молекулярної будови. Підтвердження цієї теорії з'явилися тільки в 1860-е роки, коли російський хімік Бутлеров А. М. сформував і зумів пояснити молекулярну теорію будови речовини. Згідно з його роботами властивості будь-якої речовини визначаються тим, як пов'язані між собою атоми в молекулах, їх взаємодією. Вчений висунув гіпотезу щодо того, що молекула – це мікрочастинка матеріалу, що складається з атомів, яка здатна існувати самостійно.
Вперше термін «молекула» було введено в 1811 році італійським фізико-хіміком Амедео Авогадро. Саме він став зачинателем теорії атомно-молекулярної будови. Підтвердження цієї теорії з'явилися тільки в 1860-е роки, коли російський хімік Бутлеров А. М. сформував і зумів пояснити молекулярну теорію будови речовини. Згідно з його роботами властивості будь-якої речовини визначаються тим, як пов'язані між собою атоми в молекулах, їх взаємодією. Вчений висунув гіпотезу щодо того, що молекула – це мікрочастинка матеріалу, що складається з атомів, яка здатна існувати самостійно.
Закріпилося поняття молекули завдяки працям ще одного російського вченого. Мова йде про М. в. Ломоносова. У розвитку атомістичного вчення брало участь безліч вчених з усього світу: Дж. Максвелл, Л. Больцман, Дж. Гіббс, Р. Клаузіус, Дж. Дальтон, Д. І. Менделєєв, Ст. Рентген, А. Беккерель, Дж. Томсон, М. Планк і багато інших. Внесок цих людей у молекулярну фізику та хімію безцінний. На підставі комплексу навчань за довгі роки була виведена молекулярна теорія будови речовини. Існує декілька основних положень цієї теорії, а саме три базових твердження, які були доведені неодноразово шляхом проведення лабораторних досліджень:
На підставі комплексу навчань за довгі роки була виведена молекулярна теорія будови речовини. Існує декілька основних положень цієї теорії, а саме три базових твердження, які були доведені неодноразово шляхом проведення лабораторних досліджень: Будь-яке тіло складається з найдрібніших частинок – молекул і атомів, які також складаються з більш дрібних елементів. Структура всіх речовин переривчаста. Атоми і молекули перебувають у невпинному русі хаотичної природи. Всі речовини взаємодіють між собою на підставі електромагнітних сил тяжіння і відштовхування.

Поява поняття «атомно-молекулярна будова речовини»
Ще в часи Древньої Греції з'явилася думка про те, що все на світі складається з дрібних частин. Ці частинки греки називали молекулами і атомами. Автором даної гіпотези був Демокріт, який згодом став родоначальником атомістичної теорії. Але ці знання в ті часи особливо не розвивалися аж до 17 століття. Всі дослідження матеріалів знову приводили до того, що багато речовини складаються з молекул, структурною одиницею яких є атоми. Пізніше вчені стали приходити до висновків, що один тип мінералу складається, наприклад, із заліза на 38 % і кисню на 62 %, і кожен із зразків покаже такий хімічний склад. А от якщо взяти інше тіло, з відмінними властивостями, то аналіз атомно-молекулярної будови речовини покаже, що воно складається на 60 % із заліза і на 40 % з кисню.Таким чином, незважаючи на те, що певної концепції все ж не було, в ході досліджень почала з'являтися теорія про те, що кожна речовина є різним набором молекул і атомів, які визначають його основні властивості.
Розвиток поняття «молекулярне будова речовини»
Закріпилося поняття молекули завдяки працям ще одного російського вченого. Мова йде про М. в. Ломоносова. У розвитку атомістичного вчення брало участь безліч вчених з усього світу: Дж. Максвелл, Л. Больцман, Дж. Гіббс, Р. Клаузіус, Дж. Дальтон, Д. І. Менделєєв, Ст. Рентген, А. Беккерель, Дж. Томсон, М. Планк і багато інших. Внесок цих людей у молекулярну фізику та хімію безцінний.
Суть молекулярної теорії будови речовини

Обґрунтування тез молекулярно-кінетичної теорії
Першим підтвердженням положень теорії є броунівський рух, що було відкрито в 1827 році відомим ботаніком Р. Броуном. Причина такого явища – хаотичний перебіг молекул в різних напрямках, який відбувається внаслідок ударів їх між собою. Другим підтвердженням цієї теорії будуть численні досліди з процесом дифузії, тобто здатність однієї речовини проникати в друге. Яскравим прикладом такого досвіду з повсякденного життя є духи або будь-яке запашне речовина. Якщо в приміщенні помістити таку речовину, через деякий період аромат розсіється по всій його площі.Атом і молекула
Сьогодні ці терміни вже обгрунтовані і виведені точно і аргументовано. Простою мовою, атом – це хімічно неподільна частинка будь-якої речовини або матеріалу, складова молекули. А молекула – це найменша частинка чого-небудь, але важливо те, що саме вона задає основні властивості тіла. Молекулярну будову речовини є каркасом певного матеріалу, у з'єднаннях якого знаходяться молекули. Якщо для матеріалу характерна кристалічна решітка молекулярна, то він, як правило, володіє невисокою твердістю, його легко розплавити; таке речовина буде летючим або розчинною у воді, не проводить електрику. Наука, що вивчає силу взаємодії цих частинок і молекулярну будову тіл, називається молекулярною фізикою. Тут досліджуються різноманітні властивості тіл у різних агрегатних станах.Які речовини мають молекулярну будову?
Молекулярна зв'язок, як правило, слабка і переважає в органічних речовинах. Молекулярну будову мають багато відомі нам речовини. Наприклад, вода (Н 2 Про), водень (Н 2 ), хлор (Cl 2 ), вуглекислий газ (СО 2 ), кисень (Про 2 ), етанол, або спирт етиловий (З 2 Н 5 ВІН), органічні полімери) і багато інших. Іншими словами, речовини, що мають молекулярну будову, - це в основному гази. В них молекули знаходяться далеко один від одного і взаємодіють слабо. Тісний зв'язок між частницами того чи іншого речовини утворює тверді тіла. Єдина рідина, яка має молекулярну будову, – це Br 2 . Ця речовина володіє високою летючістю. До неметаллам з молекулярною будовою відносяться такі тверді речовини, як I 2 , P 4 , S 8 . Ці матеріали легкоплавки і можуть сублимироваться.Читайте також
НАУКА
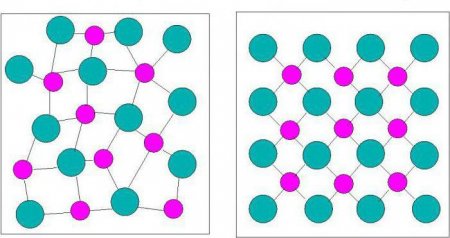
Аморфні тіла: характеристика, опис і властивості
НАУКА
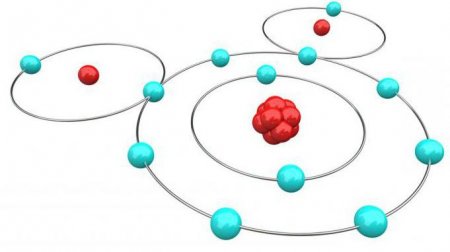
Ковалентний полярний зв'язок: формула, властивості, особливості
НАУКА
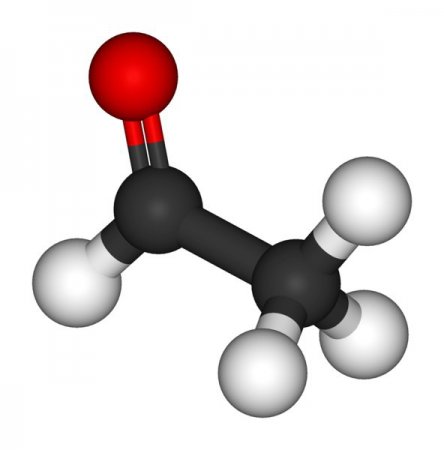
Альдегіди: хімічні властивості, одержання, будова

НАУКА
Досвід Штерна - експериментальне підтвердження теорії
НАУКА
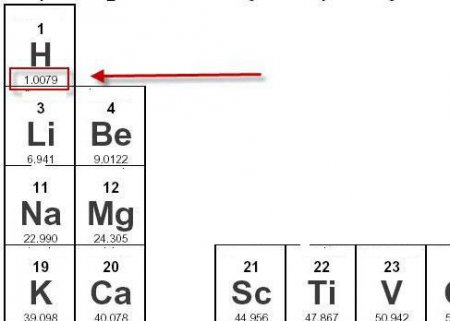
Чому дорівнює молярна маса водню?

НАУКА
Кисень: хімічні властивості елемента

НАУКА
Ідеальний газ і його визначення

НАУКА
Молекулярна маса: базові принципи визначення